北京时间2025年5月28日,珠海泰诺麦博制药股份有限公司(以下简称“泰诺麦博”)联合中国科学院上海神经科学研究所、西安交通大学,在国际高水平期刊《Cell Reports》发表重要研究成果:研究团队通过冷冻电镜在原子水平揭示了靶向人巨细胞病毒(Human cytomegalovirus, HCMV)关键膜蛋白gB的多功能高效单克隆中和抗体1B03的结合表位和作用机制 [1]。泰诺麦博开发的重组抗人巨细胞病毒(HCMV)全人源单抗药物—TNM006注射液,即是该研究论文中涉及的1B03单抗,已于2023年5月获中国国家药监局(NMPA)临床试验默示许可,成为国内首款进入临床阶段的抗HCMV单抗药物。该研究对TNM006注射液的临床开发提供了有力的科学基础和支撑。
临床需求迫切:传统疗法存在多重瓶颈
作为感染人类的八大疱疹病毒之一,HCMV是一种广泛存在于人体内的条件致病性病原体,在中国感染率达90%以上,其中一般人群HCMV抗体阳性率为86%-96%,孕妇为95%左右,婴幼儿为60%-80%[2,3]。HCMV感染是免疫抑制剂使用后出现的最常见的病毒感染,如不进行预防,高达75%的实体器官移植受者将在移植后3个月内出现新的HCMV感染或潜伏的HCMV激活,最终可导致器官移植失败乃至死亡。此外,先天性HCMV感染也是造成小儿神经性听力缺陷和小儿中枢神经系统损伤的主要原因[4]。
目前临床上用于预防和治疗HCMV感染和疾病的药物主要是小分子药物和未在国内上市的巨细胞病毒免疫球蛋白(CMV immunoglobulin, CMVIG)。因临床耐药性问题日益严峻,严重制约了小分子药物的临床使用[5]。而CMVIG受限于血浆来源短缺及病毒污染风险。因此,迫切需要一种更安全、更高效的抗HCMV单克隆抗体,以满足预防和治疗HCMV疾病这一尚未满足的临床需求。

破解临床难题:高效多功能抗体替代传统疗法
研究表明,体内HCMV主要是通过细胞间直接传播,而不是通过释放游离病毒进行传播[6,7]。因此,中和游离病毒和抑制病毒细胞间传播的生物学活性成为高效中和性抗体筛选的标准。泰诺麦博研究发现的抗HCMV天然全人源单克隆抗体,不但能广谱高效中和游离病毒,中和活性EC50值最小达到0.006 μg/mL,而且能有效抑制病毒细胞间传播(图1)[1]. HCMV以潜伏感染的形式存在于大多数的人群中, 在机体免疫低下时病毒重新激活后的传播就是以细胞间传播为主。这与抗体1B03不仅能中和血液循环中的游离病毒,还可抑制HCMV细胞间传播的双重功能特征相契合,且其双重抗病毒活性均优于目前临床阶段的同靶点抗体药物[8,9]。
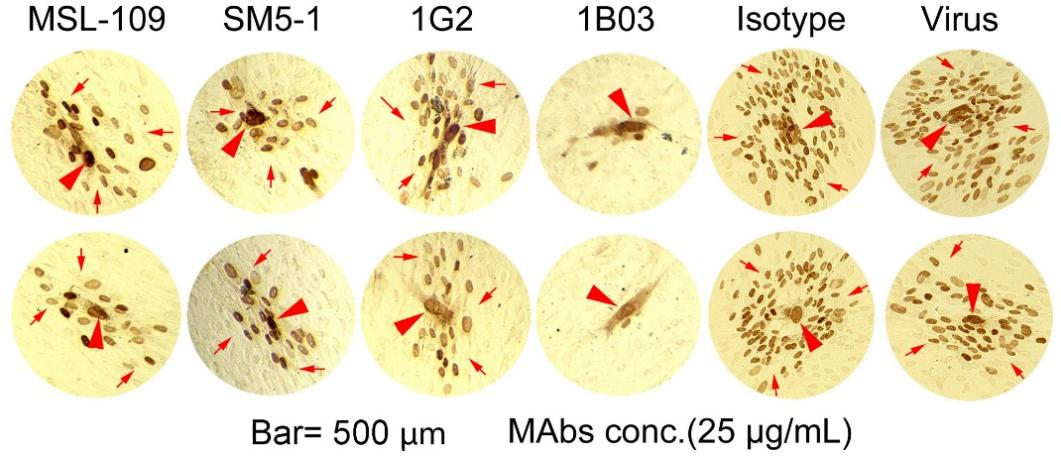
图1. 抗体1B03和对照抗体抑制病毒细胞间传播
为了阐明HCMV多功能中和抗体的作用机制,泰诺麦博联合中科院上海神经科学研究所及西安交通大学,成功解析了抗体1B03与膜蛋白gB复合物的冷冻电镜结构。研究发现,抗体1B03的结合表位显著区别于既往报道的gB靶向中和抗体,其特异性结合在gB蛋白上行使膜融合功能的关键亚结构域,通过直接阻断病毒与宿主细胞的融合过程实现高效中和(图2)。这项研究不仅从结构生物学角度揭示了抗体多功能高效中和活性的分子基础,其创新性发现为预防和治疗HCMV疾病提供了科学基础,同时为基于gB蛋白构象设计的疫苗研发开辟了新方向。
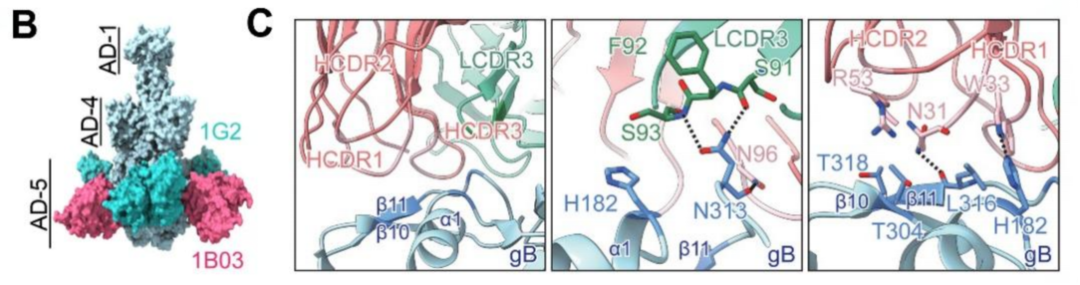
图2. HCMV gB三聚体蛋白与抗体1B03Fab复合物的冷冻电镜结构
文章作者团队由珠海泰诺麦博制药股份有限公司牵头,携手中科院上海神经科学研究所、西安交通大学,从结构上阐明了HCMV多功能中和性单克隆抗体的作用机理,为抗HCMV天然全人源单抗药物实现产业化提供了有力的科学支撑。
药物进展:全人源抗体TNM006进入临床
TNM006注射液是泰诺麦博基于第四代抗体研发技术自主研发的重组抗人巨细胞病毒(HCMV)天然全人源单克隆抗体,可最大限度地避免抗体的免疫原性和免疫反应性,其主要作用机制是特异性结合HCMV gB蛋白,抑制gB蛋白介导的膜融合功能,从而达到控制HCMV感染的目的。
相比免疫球蛋白,天然全人源抗HCMV单克隆抗体,因其具有特异性强、中和效价高、安全性好,无免疫原性等优点,在临床前药效及药理中显示出极高的病毒中和活性和良好的安全性。重组抗体是通过成熟的工业规模化生产,不仅显著降低了生产成本,而且还规避了传统免疫球蛋白的血源依赖性和传染性疾病易感风险。未来一旦上市,有望弥补小分子抑制剂的缺陷并取代HCMV免疫球蛋白,提高实体器官移植的成功率,为临床防治HCMV感染提供一项有效的手段。泰诺麦博表示,目前TNM006注射液已进入临床阶段,未来将加速推进临床试验,力争早日惠及患者,为全球抗击HCMV疾病贡献“中国智慧”。

参考文献:
[1]Changwen Wu,et al. Structural basis of human cytomegalovirus neutralization by gB AD-5-specific potent antibodies. Cell Rep. 2025,44(5).
[2]Li Z, Tang Y, Tang N, et al. High anti-human cytomegalovirus antibody levels are associated with the progression of essential hypertension and target organ damage in Han Chinese population. PloS one. 2017,12(8):e0181440.
[3]Xiang-lan Liu, Xue-ying Gu. differential diagnostic methods between primary and non-primary cytomegalovirus (CMV) infections. Chinese Journal of Reproductive Health. 2008,19:95-98.
[4]Kenneson A, Cannon MJ. Review and meta-analysis of the epidemiology of congenital cytomegalovirus (CMV) infection. Rev Med Virol. 2007,17(4):253-276.
[5]Erice A. Resistance of human cytomegalovirus to antiviral drugs. Clinical Microbiology Reviews. 1999,12(2):286-297.
[6]Sattentau Q. Avoiding the void: Cell-to-cell spread of human viruses. Nat. Rev. Microbiol. 2008,6:815-826.
[7]Jackson J.W, Sparer T. There Is Always Another Way! Cytomegalovirus’ Multifaceted Dissemination Schemes. Viruses. 2018,10:383.
[8]Pötzsch S, et al. B cell repertoire analysis identifies new antigenic domains on glycoprotein b of human cytomegalovirus which are target of neutralizing antibodies. PLoS Pathog. 2011,7(8):e1002172.
[9] Nina R,et al. Neutralizing antibodies limit cell-associated spread of human cytomegalovirus in epithelial cells and fibroblasts. Viruses. 2022,14(2):284.