2026年3月2日,由珠海泰诺麦博制药股份有限公司(以下简称“泰诺麦博”)自主研发的重组长效抗呼吸道合胞病毒(RSV)全人源单克隆抗体——芮特韦拜单抗注射液(曾用名:TNM001注射液),被正式纳入国家药品监督管理局药品审评中心(CDE)优先审评审批程序。
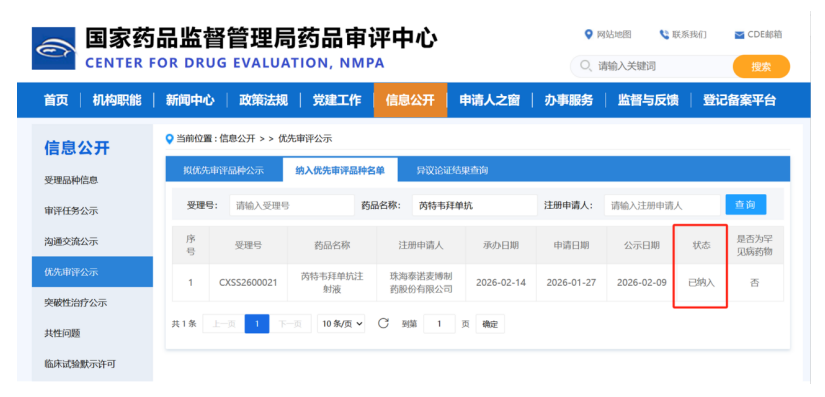
(截图来源:国家药品监督管理局药品审评中心官网)
这是继公司已上市的全球首创新一代“破伤风针”——斯泰度塔单抗注射液(商品名:新替妥)之后,泰诺麦博又一款重磅创新单抗药物获得CDE优先审评资格,充分彰显了公司在原创抗体药物研发领域的持续突破与硬核实力。依据药品审评相关规定,芮特韦拜单抗注射液上市许可申请审评时限将显著缩短,标志着这款面向健康及高危婴儿的RSV预防用长效单抗上市进程全面提速,有望更快惠及中国及全球婴儿群体!
RSV阳性率持续上升,婴儿健康主要威胁
呼吸道合胞病毒(human Respiratory Syncytial Virus, RSV)是导致5岁以下儿童下呼吸道感染(Lower Respiratory Tract Infections, LRTI)的最常见病毒病原体。全球每年约3300万例RSV相关下呼吸道感染,导致360万例住院,超10万例死亡。研究显示,1岁以下婴儿感染RSV的死亡率比感染流感病毒高约2.5倍。早产儿、低出生体重儿、先天性心脏病患儿等是感染RSV的高危人群。感染过RSV的婴儿长大后患哮喘的风险,高于没有感染过RSV的婴儿2~3倍[1]。

四大显著优势,全面升级婴儿健康守护
01更高保护
获优先审评的芮特韦拜单抗注射液,其III期临床研究显示:在健康足月儿与晚期早产儿中,给药后150天内可显著降低RSV下呼吸道感染发生率,对重症RSV下呼吸道感染的预防保护效果尤为突出。单次肌肉注射即可覆盖整个RSV流行季,便捷高效,契合婴儿防护需求。
02靶向创新
特异性靶向RSV病毒F蛋白上一个全新的融合前构象(Pre-F)保守表位,即可特异性地结合F蛋白的融合前构象的保守抗原表位。这一独特靶向创新型,体现了其潜在的临床优势,不仅增强了药物的中和效力,也为长期保护提供了可能。
03安全性好
作为重组长效全人源单抗,其抗体序列完全源自人体,能最大程度降低免疫原性风险,特别适合免疫系统未成熟的婴儿。
04一针注射
无需多次注射,仅需一针即可为婴儿提供全流行季防护,有效减轻婴儿反复接种带来的不适与哭闹,为家庭带来更便捷、更安心的守护体验。

法规体系护航,加速源创新药审评审批
芮特韦拜单抗注射液的优先审评获批,得益于我国为鼓励药品创新、守护公众健康所不断完善的法规政策体系。新修订的《中华人民共和国药品管理法实施条例》(以下简称《条例》)[2]从行政法规层面系统性确立了突破性治疗药物、附条件批准、优先审评审批、特别审批四条药品加快上市注册路径,构建起以临床价值为导向、高效规范的现代化药品审评审批体系。
通过优先审评认定,可以加速芮特韦拜单抗注射液上市进程,既是泰诺麦博研发实力与创新能力的充分体现,更是我国生物医药产业迈向高质量发展的生动缩影。有望为中国乃至全球婴儿,在整个RSV流行季提供安全、便捷、长效的免疫保护,助力守护儿童健康。
参考文献:
[1]上海市卫生健康委员会 上海市中医药管理局《重视预防,避免呼吸道合胞病毒感染》.https://wsjkw.sh.gov.cn/crbfz/20230918/f6d65f94cbf747f4a69620e0e5db38c5.html.2023.9.18
[2]中华人民共和国中央人民政府《中华人民共和国药品管理法实施条例》(以下简称《条例》).https://www.gov.cn/zhengce/zhengceku/202601/content_7056256.htm.2026.1.16.
(以上图片均由AI生成)